Zolfo
Estrazione dello zolfo
I metodi principali di estrazione dello zolfo sono la fusione e la distillazione del materiale grezzo.
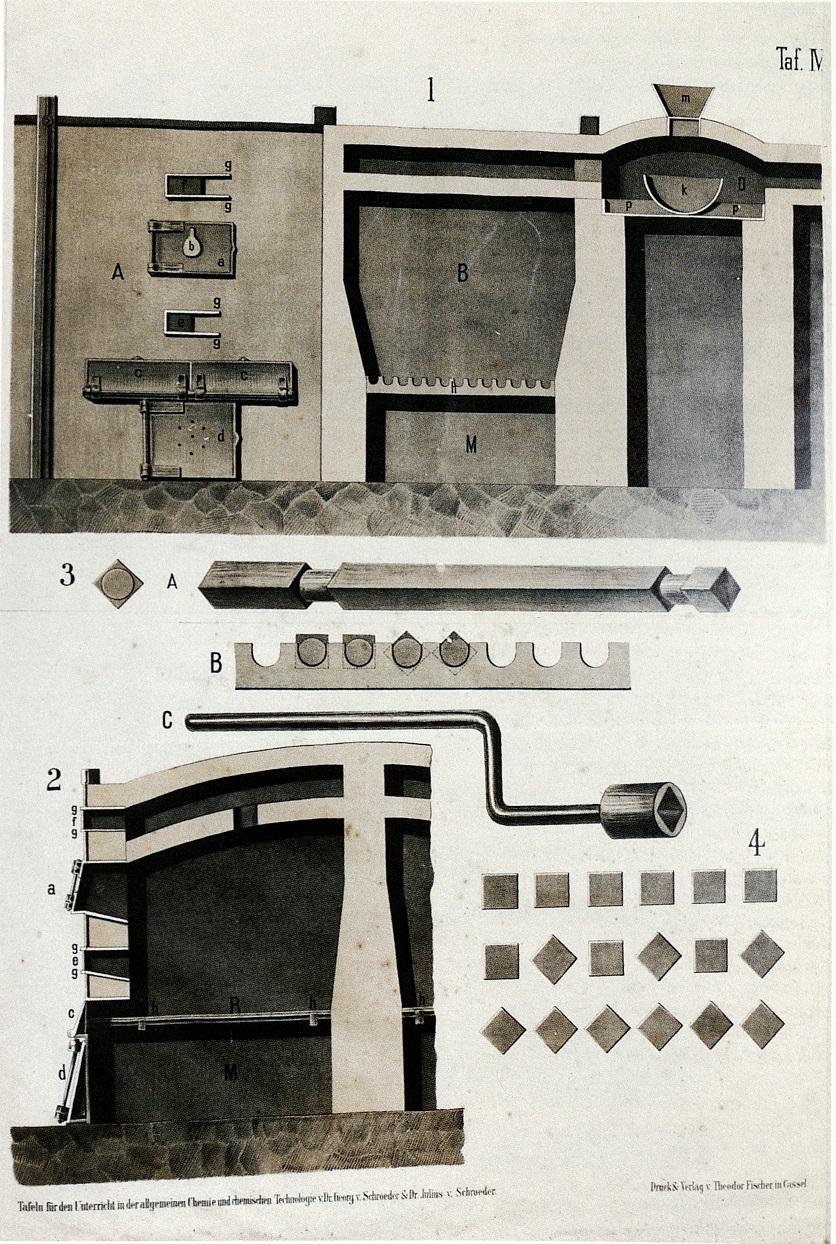
Dal 1850 lo zolfo fu prodotto con il metodo detto del calcarone (fig. 1): in una grande camera cilindrica (200-1000 mc) lo zolfo grezzo veniva stipato e ricoperto con uno strato di materiali esauriti (D) provenienti dalle precedenti lavorazioni.
Con questo metodo la combustione di una parte dello zolfo forniva il calore necessario per fondere la parte restante che veniva raccolta in forma liquida (R). Le rese erano del 60-65%.
Per distillazione (fig. 2), lo zolfo veniva ottenuto allo stato liquido (L) da rocce che lo inglobavano. Il materiale grezzo (G) era preriscaldato dai gas caldi generati dalla fornace (F) prima di essere cariato nella storta (A) all'inizio di ogni ciclo. Dato che la storta (A) era a chiusura ermetica, non si avevano perdite di zolfo per combustione, né conseguentemente inquinamento atmosferico.
Processi moderni: zolfo
L'importanza dello zolfo come materia prima dell'industria chimica è andata aumentando durante tutto il secolo XX. Il suo maggiore consumo è sempre stato quello correlato con la produzione di anidride solforosa, materia prima per la produzione di acido solforico. Lo zolfo non si estrae più, tuttavia, da miniere del tipo “siciliano”, ormai non competitive dal punto di vista economico, e pertanto anche il sistema del calcarone è andato in disuso. I giacimenti di zolfo vengono adesso sfruttati con il metodo Frasch, che usa una sonda a tre tubi concentrici. Uno di esse serve per iniettare nello strato di minerale acqua surriscaldata sotto pressione: si provoca così la fusione dello zolfo (lo zolfo fonde a 113 °C), che si raccoglie attorno all'estremità della sonda. L'immissione di aria a pressione dal secondo dei tubi concentrici provoca la risalita dello zolfo fuso in superficie attraverso il terzo tubo. Molto dello zolfo in commercio proviene dagli impianti di desolforazione dell'industria petrolifera e carbonifera. La purificazione dello zolfo viene invece ancora fatta per distillazione con impianti che, concettualmente, non differiscono da quelli illustrati nelle tavole 1 e 2.
Tecnologie antiche: zolfo
Lo zolfo ha avuto nell'antichità quasi soltanto usi di guerra: molti documenti, sia asiatici che circum mediterranei, descrivono proiettili e battelli incendiari, frecce infuocate e gas asfissianti. Fino alla scoperta della dinamite il principale uso dello zolfo fu la fabbricazione della polvere pirica scoperta dai cinesi nel IX secolo d.C. Nell'ottocento, con la nascita dell'industria chimica, il principale uso dello zolfo divenne la produzione di anidride solforosa impiegata nella produzione di acido solforico e come sbiancante nell'industria tessile. Le stesse destinazioni aveva l'anidride solforosa ottenuta per arrostimento delle piriti.
Purificazione dello zolfo
Le impurezze contenute nello zolfo grezzo ottenuto per fusione o per distillazione venivano eliminate con una ulteriore distillazione. L'impianto della tav. II funzionava in continuo: lo zolfo grezzo veniva fuso nel recipiente (K), scaldato dai gas di combustione proveniente dalla fornace (f). Per apertura del rubinetto (R), lo zolfo fuso era poi travasato dal recipiente (K) nella storta (A), dove veniva portato all'ebollizione: i suoi vapori erano quindi condensati nella camera (B), dal cui fondo veniva prelevato lo zolfo puro allo stato liquido. In ventiquattro ore si ottenevano circa 1800 kg di zolfo.
Preparazione dell'anidride solforosa: forni per piriti in pezzi grossi
L'anidride solforosa veniva prodotta industrialmente come intermedio per preparare acido solforico. Alcuni processi utilizzavano come materiale di partenza lo zolfo.
L'impianto illustrato dalla tav. IV entrò in funzione nel 1840. Con esso si produceva anidride solforosa (SO2) per arrostimento in corrente d'aria della pirite (FeS) o della sfalerite (ZnS).
La tavola mostra (in fig. 1) una vista frontale (A), la sua sezione (B) e la sezione trasversale di un forno (in fig. 2). I minerali, introdotti dalle porta (a), venivano arrostiti nelle camere (B) chiuse in basso dalle griglie (RR), al di sotto delle quali erano le fornaci (M). Per semplice rotazione degli elementi delle griglie (vedi figg. 3 e 4) in (M) venivano raccolti anche gli ossidi di ferro (o di zinco) ad arrostimento completato. Numerosi forni in batteria lavoravano alternativamente garantendo un flusso continuo di SO2 alle camere di piombo. Qui il gas arrivava attraverso il condotto (D) dopo essersi arricchito di ossidi di azoto prodotti nel reattore (K) da una miscela di acido solforico (H2SO4) e nitrato di potassio (KNO3).
Preparazione dell'anidride solforosa: forni per piriti in pezzi piccoli
L'utilizzazione della pirite in piccoli pezzi per la produzione di anidride solforosa fu resa possibile utilizzando i forni di Maletra illustrati talla tav. V in due sezioni ortogonali.
Con questo nuovo procedimento il minerale combusto conteneva al massimo l' 1-2% di pirite non arrostita.
Le lastre di terra cotta (a-f) venivano caricate con la pirite in strato sottile attraverso le porte (g), (h) ed (i). Il calore sviluppato dalla combustione del carbone posto sulla griglia (r) riscaldava il forno al calore bianco. Iniziava quindi l'arrostimento per introduzione di aria.
I gas solforosi venivano inviati alle camere di piombo.
Gli ossidi di ferro si raccoglievano nell'ambiente (q). Il soffitto della camera (m) era rivestito con una lastra in ghisa (u) su cui erano poste le capsule in piombo (v), dove l'acido delle camere era concentrato fino a 60 °C Baumé.
Processi moderni: anidride solforosa
I processi chimici per la produzione dell'anidride solforosa non hanno subito innovazioni rispetto a quelli ottocenteschi. Sono ancora:
combustione dello zolfo;
arrostimento di solfuri metallici (pirite, sfalerite, falena, blenda).
Sono stati invece profondamente innovati gli impianti. Quelli descritti nelle Tavole 4 e 5 sono impianti discontinui di arrostimento di piriti. Il loro uso prevedeva che gli addetti sorvegliassero a vista per giudicare la completezza dell'arrostimento. Le operazioni di carica e scarica erano eseguite a mano in un ambiente spesso saturo di vapori solforosi.
Gli impianti moderni lavorano in continuo: la pirite in polvere è introdotta nel reattore dall'alto, mentre dal basso arriva una corrente di ossigeno ad alta temperatura.
Le reazioni sono tanto più rapide quanto più finemente è stata polverizzata la pirite. Il reattore è collegato ad un separatore ciclonico dove gli ossidi metallici sono separati dall'anidride solforosa, che viene inviata agli impianti di produzione dell'acido solforico.