Fosforo
Preparazione del fosforo
La fig. 1 rappresenta l'apparecchiatura usata per la preparazione del fosforo bianco, costituita da una serie di storte in materiale refrattario (A), riscaldate in una fornace (B).
Nelle storte avveniva la reazione 2Ca(PO3)2 + 10C + 2SiO4 → 2CaSiO3 + 10CO +P4
Il fosforo formatosi gorgogliava attraverso tubature di rame (R) in recipienti contenenti acqua fredda, dove i suoi vapori condensavano.
La fig. 2 rappresenta l'apparecchiatura per la preparazione del fosforo rosso partendo dal fosforo bianco.
La trasformazione avveniva a 290 °C nell'autoclave di porcellana (H), scaldata indirettamente dalla fornace (R) attraverso un bagno di lega Sn/Pb al 50% (B) ed un bagno di sabbia (C).
I gas in uscita dalla caldaia venivano fatti gorgogliare nel recipiente (G) pieno di acqua o di mercurio. Il tubo di collegamento (E) era scaldato in (F) per impedire che fosse ostruito per condensazione dei vapori di fosforo. Il riscaldamento della caldaia (H) era continuato finché, dopo espulsione di tutta l'aria, dal rubinetto (h) iniziavano ad uscire vapori di fosforo (infiammabili all'aria). Il rubinetto, a questo punto, veniva chiuso e l'apparecchiatura si lasciava raffreddare fino a poter estrarre il fosforo dalla caldaia H.
Fosforo e carburo di calcio
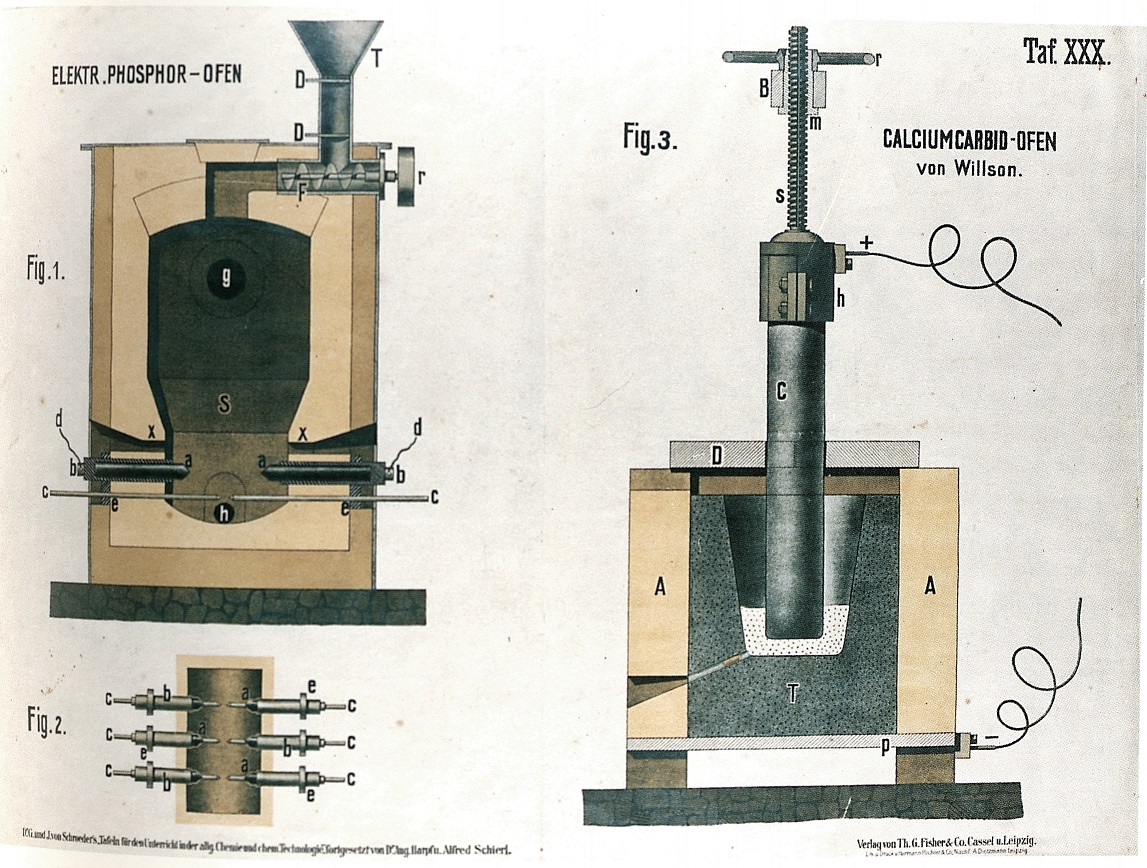
Nel forno elettrico Readman e Parker della fig. 1 avveniva il processo
Ca3(PO4)2 +14C → 3CaC2 + 8 CO + P2
L'impianto funzionava in continuo rifornito dalla miscela di partenza attraverso la tramoggia (T) e la coclea (F). Il fosforo distillava dall'apertura (g) a 1150 °C. Dall'apertura (h) venivano prelevate le scorie costituite soprattutto da carburo di calcio, CaC2. La fig. 2 mostra un dettaglio in pianta degli elettrodi (b).
Il carburo di calcio era preparato nel forno elettrico di Wilson, fig. 3, a partire da una miscela di ossido di calcio e catrame (attualmente si usa carbonio): la reazione 2CaO + 6C → 2CO + 2CaC2 decorre alla temperatura dell'arco elettrico, che scocca fra il crogiolo (F) e l'elettrodo (C), entrambi di grafite.
Processi moderni
Il fosforo bianco si prepara tuttora in fornaci elettriche. Gli impianti moderni usano corrente trifase e gli elettrodi di carbone sono disposti verticalmente ai vertici di un triangolo equilatero a breve distanza dal fondo della fornace, anch'esso di carbone. Particolare cura è dedicata alla granulazione del materiale di partenza: il fosfato tricalcico, la silice ed il carbone. Essi devono avere la stessa granulazione e devono essere distribuiti in modo omogeneo, così da avere la stessa permeabilità ai gas prodotti (CO e fosforo) in tutta la massa di reazione. Qualsiasi disomogeneità provoca infatti disomogeneo consumo degli elettrodi, differenze di resistenza elettrica e di temperatura nella massa di reazione, intasamenti ed aumenti di pressione.
Inconvenienti che si traducono in aumenti dei costi di manutenzione.
Fosforo rosso: il principale inconveniente dell'impianto ottocentesco illustrato nella tavola 19 era il fatto che il fosforo rosso si otteneva sotto forma di una massa dura e compatta che poneva problemi anche per lo svuotamento del reattore. I processi moderni usano reattori cilindrici, rotanti sull'asse cavo orizzontale, al cui interno piccole sfere di acciaio frantumano la massa di reazione. Il fosforo rosso è ottenuto così in forma polverosa.