Cloruro di sodio
Salina
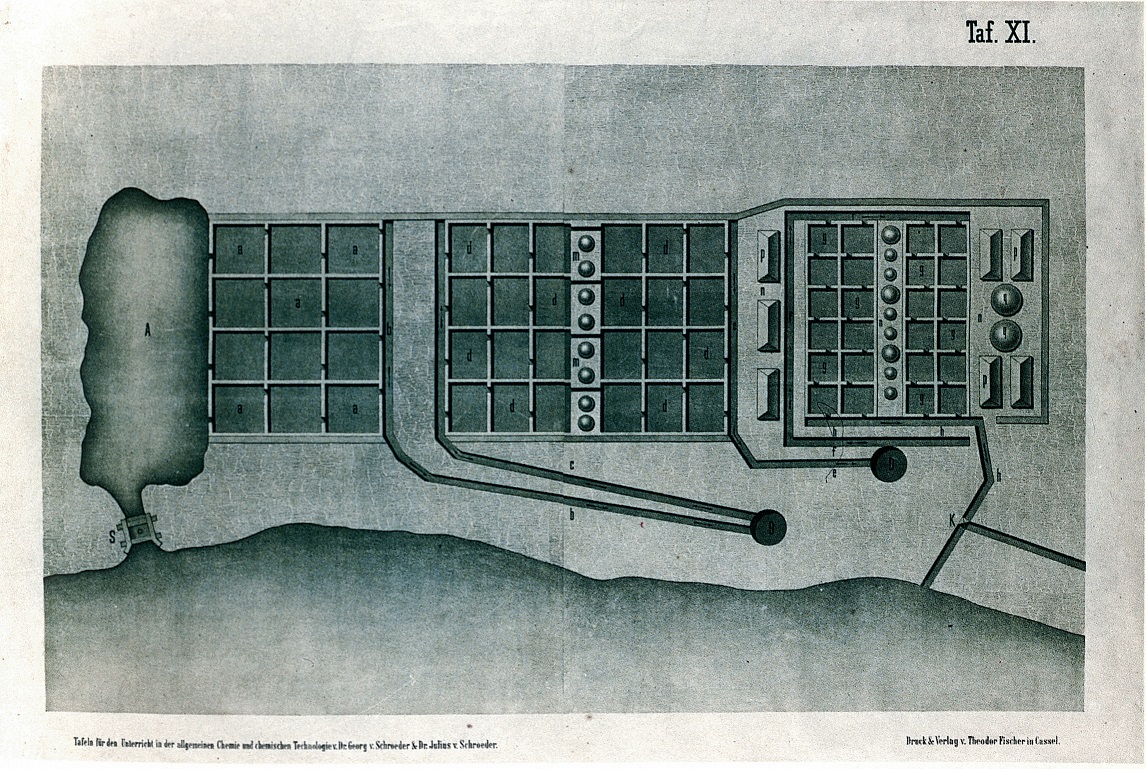
La produzione di cloruro sodico (NaCl) dall'acqua di mare è basata sul processo di evaporazione in bacini detti saline. Nel bacino (A) l'acqua di mare decanta per alcuni giorni le sue impurezze solide ed inizia ad evaporare. Viene quindi travasata nelle vasche successive, dove dapprima precipita il solfato di calcio (vasche a, d) e quindi il cloruro di sodio (vasche g), sotto forma di grandi croste cristalline. Il sale ancora umido viene raccolto in grandi cumuli (p), dove perde le acque madri molto ricche di cloruro di magnesio. Queste acque madri vengono riportate al mare attraverso il canale (h).

Apparecchio di graduazione del sale
Per concentrare l'acqua salata venivano usati anche sistemi differenti dalle vasche di evaporazione. Ad esempio, apparecchi come quello della tav. XII, detto apparecchio di graduazione. La soluzione da concentrare, posta nel serbatoio (A), percolando lentamente sulle pareti di fascine B depositava i sali di calcio poco solubili. Veniva quindi raccolta nella vasca di evaporazione (C). Un particolare dispositivo (figg. 3-4) consentiva di far gocciolare l'acqua su un lato o sull'altro dell'apparecchio di graduazione, a seconda della direzione prevalente del vento.
Raffinazione del sale
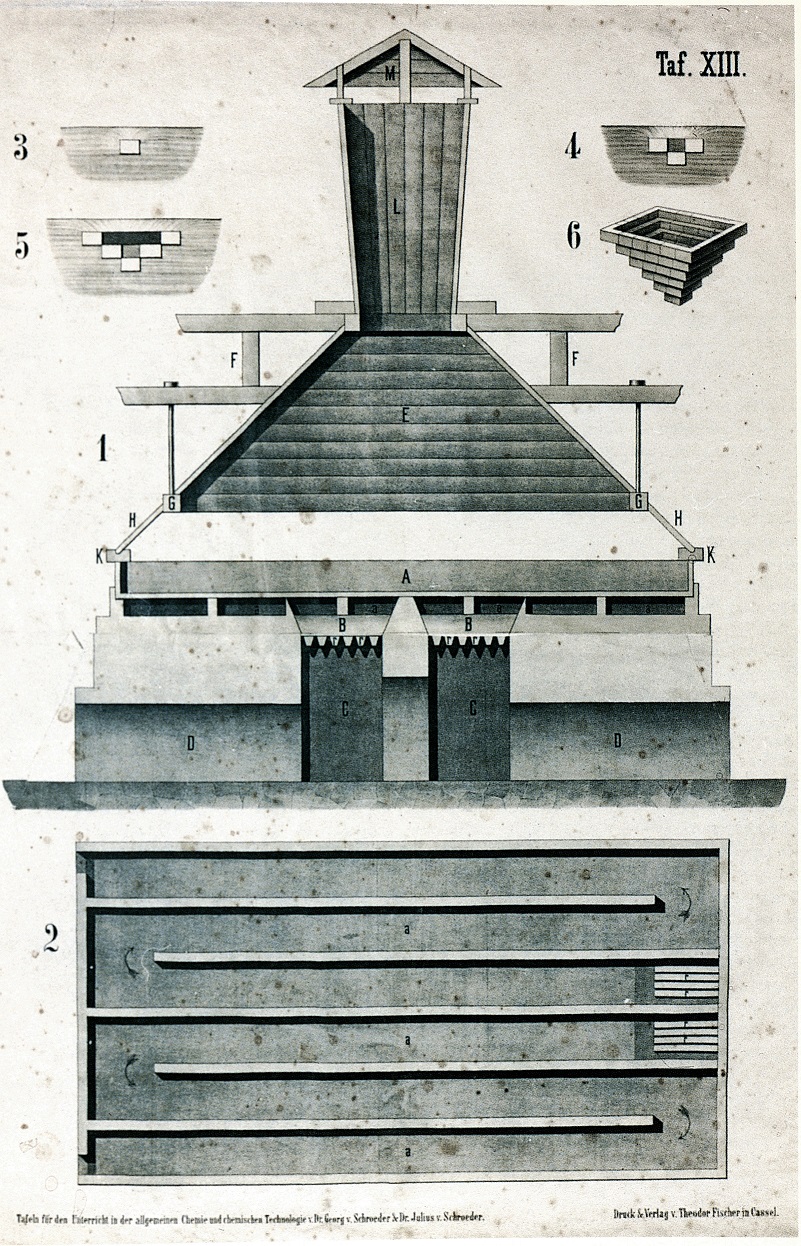
La tavola XIII rappresenta in sezione (1) ed in pianta (2) un'apparecchiatura per la cristallizzazione del cloruro di sodio (NaCl). L'operazione era eseguita in una grande capsula di ferro (A), nella quale una soluzione acquosa diluita di sale da purificare evaporava per riscaldamento. La capsula poggiava sui canali (a) dei gas di combustione prodotti nelle due fornaci (B), fornite, queste, di ceneratori (C) ed aerate attraverso le condotte (D). La cappa (f) garantiva il tiraggio del vapor d'acqua. La soluzione, durante l'evaporazione, era agitata attraverso le feritoie apribili (K), che servivano anche per estrarre con grandi pale il CaSO4 ed il Na2SO4, i primi a cristallizzare. Continuando l'evaporazione, sulla superficie del liquido cristallizzava il NaCl sotto forma di piccoli cubi galleggianti. Ai quattro lati di ciascun cubetto se ne formavano altri quattro, e la piccola piramide cominciava ad affondare.
Il processo continuava dando origine a strutture cristalline a forma di piramide cava (figg. 3-6). Il sale veniva raccolto attraverso le feritoie (K) e messo a sgocciolare in grandi ceste.
Processi moderni
Il cloruro sodico è la materia prima di quasi tutti i composti che contengono Sodio o Cloro.
Attualmente soltanto il 50% del sale in commercio deriva dall'evaporazione solare, il resto è di origine mineraria (salgemma). I giacimenti vengono coltivati iniettando acqua nello strato minerale ed estraendone salamoia. L'operazione è condotta usando una sonda a due tubi concentrici, uno per la mandata di acqua e l'altro per il ritorno della soluzione salina. Quest'ultima viene filtrata ed evaporata fino a cristallizzazione.
Il salgemma pone minori problemi di purificazione del cloruro sodico proveniente dalle saline. Infatti, i depositi del minerale si sono formati in epoche geologiche remote per lenta evaporazione di bacini marini. Si ebbe un vero processo di cristallizzazione frazionata dei sali contenuti nell'acqua di mare. I primi a cristallizzare erano i sali meno solubili e via via tutti gli altri.
Il salgemma usato per scopi alimentari deve essere addizionato di ioduri, mentre il cloruro sodico da salina li contiene come impurezza.
Tecnologie antiche
Il cloruro sodico ha un posto importante nella storia dell'uomo: gli ha consentito di conservare il cibo e di trasportarlo in luoghi distanti dal luogo di produzione. Per questo era oggetto di commercio intenso fra le popolazioni costiere e quelle dell'interno.
La concia delle pelli era un altro impiego importante del sale. Gli unici che siano riusciti, fin dall'antichità, a prescindere dai rifornimenti di sale marino sono stati i cinesi: essi sfruttavano i giacimenti di salgemma pompando acqua ed estraendo salamoia attraverso due tubi concentrici di bambù. Le salamoie erano poi concentrate bruciando gas naturale sotto grandi caldaie di bronzo.